
Diferenças entre medicamentos de Referência, Genéricos e Similares: O que você precisa saber sobre qualidade e troca segura
Entender a diferença entre os medicamentos é importante na hora da escolha do tratamento com seu médico. Leia o blogpost a seguir.
Você já esteve na farmácia com uma receita médica e o farmacêutico sugeriu um genérico ou similar em vez do medicamento prescrito pelo seu médico? Isso é o que chamamos de intercambialidade de medicamentos, uma prática respaldada por regulamentos de saúde que permitem a substituição de medicamentos por opções equivalentes.1,2
Neste artigo, vamos explicar tudo o que você precisa saber sobre intercambialidade de medicamentos e como isso pode afetar suas escolhas na hora de comprar remédios na farmácia.
O que são medicamentos de Referência, Genéricos e Similares?
No mercado, existem diferentes tipos de medicamentos: os de Referência, os Genéricos e os Similares. É essencial entender as distinções entre eles para saber sobre a qualidade de cada medicamento e quanto é possível fazer uma troca segura.1,2
- Medicamento de Referência: É o medicamento original desenvolvido por uma empresa farmacêutica. Ele passa por extensos estudos para comprovar sua eficácia, segurança e qualidade antes de ser aprovado para uso.1,2
- Medicamento Genérico: É uma versão do medicamento de referência, contendo o mesmo princípio ativo em igual dosagem. Ele não tem nome comercial e é vendido com o nome do princípio ativo (substância que produz os efeitos terapêuticos). Sua embalagem sempre traz escrito: “Medicamento Genérico – Lei 9.787/99” e uma tarja amarela com a letra G de genérico. É geralmente mais barato porque não requer os mesmos testes de eficácia e segurança que o referência. Porém só pode substituir o medicamento de referência após passar por testes laboratoriais que comprovem sua equivalência.1
- Medicamento Similar: Também contém o mesmo princípio ativo em igual dosagem, porém pode ter diferenças em alguns aspectos, como prazo de validade, embalagem, rótulo, tamanho e forma. Ele tem um nome comercial diferente. É geralmente mais barato porque não requer os mesmos testes de eficácia e segurança que o referência. Porém só pode substituir o medicamento de referência após passar por testes laboratoriais que comprovem sua equivalência, da mesma forma que os genéricos, quando isso acontece passam a ser chamados de similares bioequivalentes.2
O que é intercambialidade de medicamentos?
Intercambialidade de medicamentos refere-se à possibilidade de trocar um medicamento de referência por um similar ou genérico. Para que essa troca seja segura, é necessário que o medicamento similar ou genérico tenha passado por testes de bioequivalência em indivíduos saudáveis.1-4
Estes testes comparam dois medicamentos que têm o mesmo princípio ativo, mostrando a rapidez e a quantidade que o corpo absorve de cada um dos medicamentos. Sendo útil para entender como os medicamentos se comportam no organismo e verificar se os níveis de concentração desses medicamentos no corpo são semelhantes o suficiente para serem considerados intercambiáveis.3
Para que dois medicamentos sejam considerados bioequivalentes, a absorção e a velocidade da absorção devem ser semelhantes entre os medicamentos comparados. Dessa forma é possível garantir que o efeito desses medicamentos seja similar.3
Não é possível garantir que o efeito será igual, pois a biodisponibilidade média de genéricos e similares pode variar de 80%-125% da biodisponibilidade média do medicamento referência por lei³.
Embora pareça complicado, é muito importante seguir as regras legais para garantir que os medicamentos sejam seguros e eficazes. Quando os medicamentos funcionam conforme esperado, eles podem ajudar a resolver os problemas de saúde dos pacientes.3
Quais medicamentos são intercambiáveis?
Veja abaixo uma figura que exemplifica quais são as trocas possíveis entre medicamentos (Figura 1):5
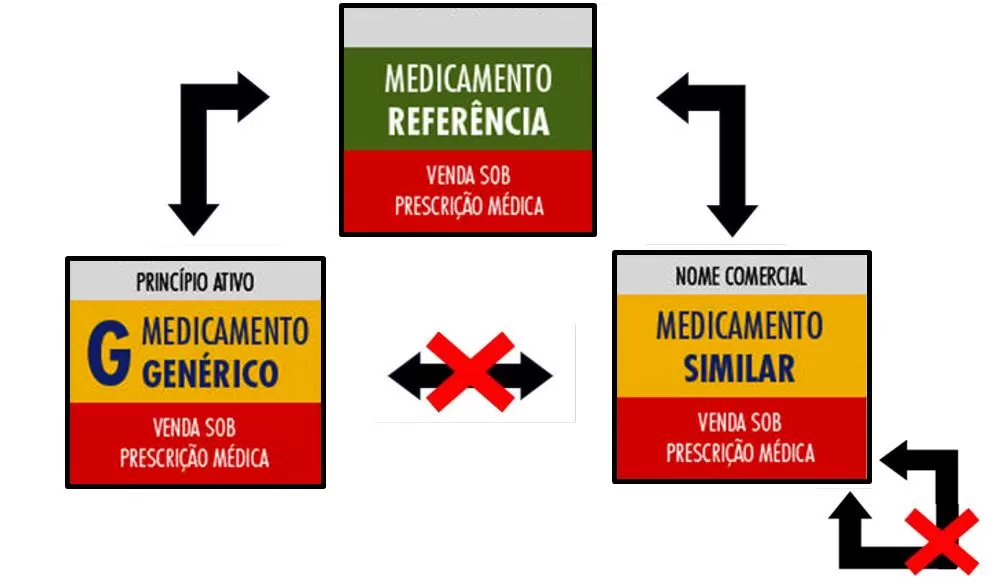
Figura 1. Intercambialidade de medicamentos.
Adaptada de Anvisa, 2024.5
Se o médico prescrever um medicamento similar, não é permitido substituí-lo por um genérico na farmácia, de acordo com a legislação. De acordo com a RDC 58/2014, a troca entre um medicamento similar e um genérico não é permitida pela legislação.5
A legislação atual permite apenas a troca entre medicamento genérico e seu medicamento de referência correspondente, assim como entre medicamentos similares e seus medicamentos de referência. A RDC 58/2014 não autoriza a substituição entre medicamentos similares ou entre similares e genéricos 5.
A Anvisa autoriza o intercâmbio de medicamentos somente nos seguintes casos: ⁵,⁶
Medicamento de Referência
Se o médico receitar um medicamento de referência, você pode comprar o próprio medicamento de referência, um similar intercambiável ou um genérico. ⁵,⁶
Medicamento Genérico
Se a receita contiver apenas o princípio ativo e sua concentração, o farmacêutico pode lhe fornecer um medicamento genérico de qualquer fabricante, ou o medicamento de referência. No entanto, o medicamento similar não pode ser dispensado nesse caso. ⁵,⁶
Medicamento Similar
Se o médico prescrever um medicamento similar, o farmacêutico pode fornecer o medicamento similar mencionado na receita ou o medicamento de referência. ⁵,⁶
É importante observar que, nos três casos acima, se o médico indicar na receita que não deve haver substituição do medicamento prescrito, as regras mencionadas acima não se aplicam. Nesse caso, o farmacêutico deve fornecer exatamente o medicamento especificado na receita médica, sem fazer substituições. ⁵,⁶
Se tiver dúvidas sobre algum medicamento, sempre consulte seu médico ou farmacêutico. Eles podem ajudar a esclarecer qualquer questão e garantir o uso correto e seguro dos medicamentos.
O que pode acontecer se ocorrer um intercâmbio indevido?
A troca indevida de medicamentos pode afetar o tratamento, fazendo com que os resultados não sejam o esperado (menor eficácia e/ou mais efeitos adversos).6
Referências Bibliográficas
1. Brasil, Presidência da República. Lei no 9.787, de 10 de fevereiro de 1999. Altera a Lei no 6.360, de 23 de setembro de 1976, que dispõe sobre a vigilância sanitária, estabelece o medicamento genérico, dispõe sobre a utilização de nomes genéricos em produtos farmacêuticos e dá outras providências. Brasília: Diário Oficial da União (DOU); 11 Fev 1999. Seção 1, 4 p.
2. Lima RQ, de Almeida MCP, Farias Jr ENF, Lima Neto LS. Intercambialidade entre medicamentos de referência e similar . Braz J Dev. 2020;6(12):101122-32.
3. Araújo LU, Albuquerque KT, Kato KC, Silveira GS, Maciel NR, Spósito PA, et al. Medicamentos genéricos no Brasil: panorama histórico e legislação. Rev Panam Salud Publica. 2010;28(6):480-92.
4. Ministério da Saúde, Agência Nacional de Vigilância Sanitária. Resolução no 391, de 9 de agosto de 1999 [acesso em 2020 Ago 4]. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/anvisa/1999/res0391_09_08_1999….
5. Agência Nacional de Vigilância Sanitária (Anvisa). Medicamentos similares. 2024. Disponível em: <https://www.gov.br/anvisa/pt-br/assuntos/medicamentos/similares>. Acesso em abril de 2024.
6. Memed. O que é intercambialidade de medicamentos? Saiba quando trocar medicamentos de referência por similares e genéricos. Disponível em: <https://blog.memed.com.br/o-que-e-intercambialidade-de-medicamenos/>. Acesso em abril de 2024.
PP-PRQ-BRA-1029 - Março 2026.